GR (RECEPTOR DE GLUCOCORTICOIDES)
RECEPTORES NUCLEARES
Los receptores de glucocorticoides (GRs) están codificados por el gen NR3C1 y pertenecen a la subfamilia de receptores de hormonas esteroideas, junto con los receptores de estrógenos (ERs), andrógenos (ARs), progesterona (PRs) y mineralocorticoides (MRs) (Cohen&Steger, 2017).
Ligandos
Los ligandos de los GRs son los glucocorticoides (GCs), un tipo de hormona esteroidea sintetizado en la corteza suprarrenal; el término GCs refleja su propiedad reguladora de la glucosa (glucosa), su lugar de producción (córtex) y su composición estructural (esteroide). Los GCs son moléculas de naturaleza lipofílica, cuyo origen puede ser endógeno o sintético, y que interaccionan con los GRs a través de su dominio de unión a ligando (dominio E) regulando las acciones fisiológicas y/o farmacológicas de los GRs (Timmermans et al. 2019; Vandevalle et al. 2018).
Clasificación
Los GRs son miembros de la subfamilia NR3 de la superfamilia de receptores nucleares (NRs).
A su vez, en base a su afinidad por el ligando y a su modo de acción, se clasifican como receptores «endocrinos» y de Tipo I.
Estructura e interacciones
Todos los miembros de la familia de receptores nucleares comparten una estructura general en multidominio. En concreto, los GRs son similares a otros receptores de hormonas esteroideas, estando constituidos por los siguientes dominios:
- Dominio A/B (NTD / AF-1): región de unión a coactivadores en posición N-terminal, con función de transactivación del DNA (AF-1), pudiendo operar de forma dependiente o independiente del ligando.
- Dominio C (DBD): región de unión al DNA altamente conservada, que contiene dos «dedos de zinc» que interactúan con los elementos de respuesta hormonal específicos (motivos HREs, en este caso denominados GREs), y de mediación de la dimerización del receptor.
- Dominio D o “región bisagra”: región de unión de los dominios C y E, y que da flexibilidad al receptor.
- Dominio E/F (LBD / AF-2): región de unión al ligando y de interacción con los coactivadores y corepresores (función de transactivación AF-2 dependiente de ligando), en posición C-terminal.
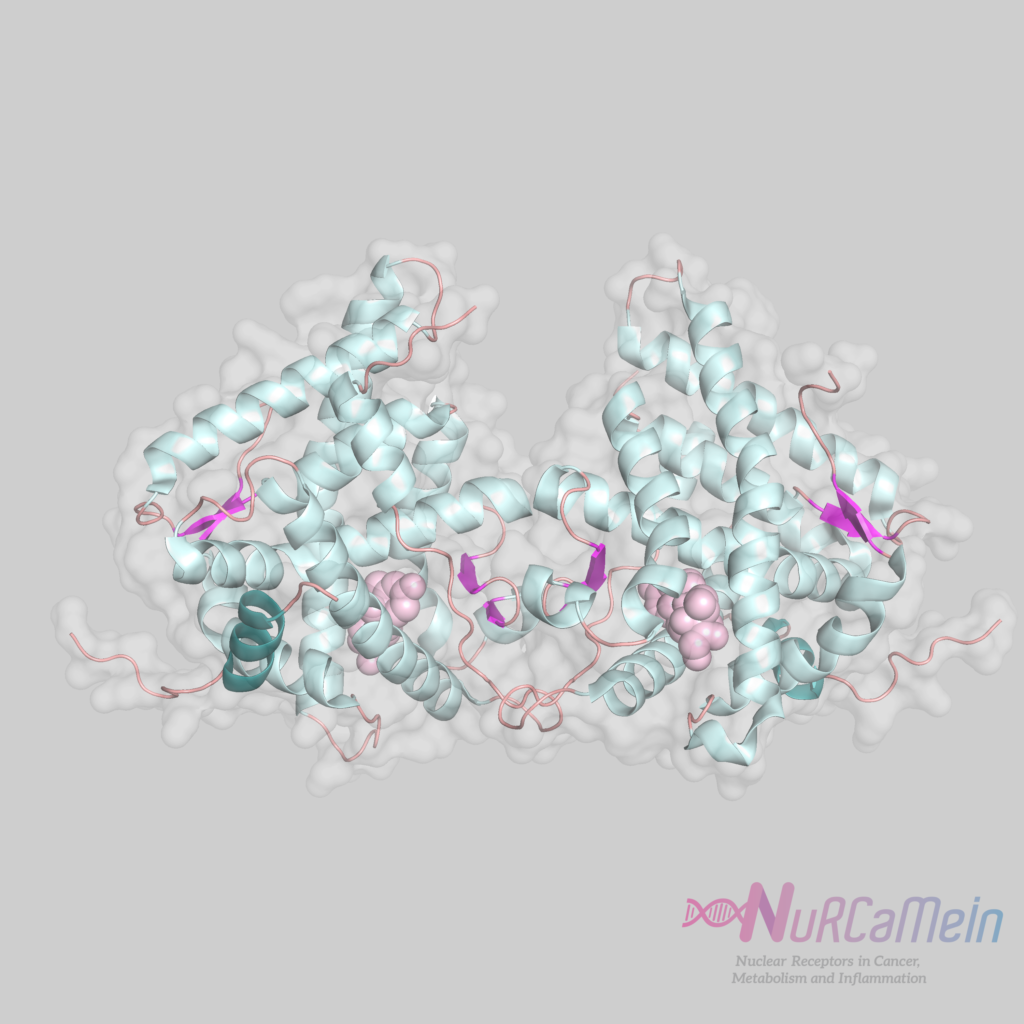
Estructura del GR
En respuesta a los GCs, los GRs regulan la transcripción de sus genes diana, mediante mecanismos genómicos y no genómicos (Cohen&Steger, 2017; Weikum et al. 2017).
En ausencia de GCs, los GRs se hallan en el citoplasma unidos a un complejo de proteínas chaperonas (hsp o heat-shock proteins e inmunofilinas). Tras la unión del GC, el complejo experimenta un cambio conformacional que induce la entrada del GR/GC al núcleo, donde ejercen su actividad transcripcional, pudiendo ser de activación o repression génica
Estudios recientes en células vivas muestran que los GRs pueden formar distintos oligómeros, incluidos dímeros y tetrámeros, mediante interacciones alostéricas con el DNA. Los distintos estados de oligomerización de los GRs pueden ser determinantes en la regulación de la expresión génica en respuesta a hormona (Jiménez-Panizo et al. 2022).
Los GRs regulan la transcripción de sus genes diana de tres maneras principales:
- Unión directa a secuencias GREs (secuencia consenso AGAACAnnnTGTTCT), que resulta en el reclutamiento de coreguladores y activación de la transcripción; o secuencias negativas nGREs (CTCC(n)0–2GGAGA), que resulta en el reclutamiento de corepresores e inhibición de la transcripción.
- Interacción física con otros factores de transcripción, que altera sus capacidades transcripcionales, sin requerir la unión directa del GR al DNA.
- Unión a «elementos compuestos» o secuencias de DNA que contienen tanto GREs como elementos de respuesta a otros factores de transcripción; este tipo de regulación puede resultar tanto en activación como en represión de la expresión génica.
Los GRs también puede formar heterodímeros con el receptor de mineralocorticoides (MR)), confiriendo al complejo la capacidad de regular la especificidad y la magnitud de la respuesta transcripcional a GCs transcripción génica de una forma única para ambos tipos de receptors (Carceller et al. 2023).
Los GCs pueden llevar a cabo su acción de forma mucho más rápida (en minutos en lugar de horas) a través de la vía no genómica (no requiere cambios transcripcionales), activando una cascada de señales que se desencadena tras su unión a los GRs presentes en la membrana celular o en el citoplasma (Bruna et al. 2003).
Expresión
NR3C1 es un genque codifica para distintas isoformas de GR, que difieren en sus extremos N- o C-terminal (Ramamoorthy &Cidlowski, 2016), La isoforma más abundante en la mayoría de tipos celulares es GRa, capaz de unir ligando y regular la expresión génica. Además, existen otras isoformas entre las que destaca GRβ ya que, a diferencia de GRα, no se une a los GCs y tiene la capacidad de inhibir la actividad de GRα a través de diferentes mecanismes. Por ello, un alto nivel GRβ puede dar lugar a resistencia a los GCs.
A pesar que los GRs se expresan de forma ubicua en el organismo, su actividad transcripcional es específica de tipo celular, probablemente debido a interacciones selectivas con coreguladores específicos.
Principales funciones
La función de los GCs y, por ende, de los GRs es de gran importancia para la fisiología humana, ya que regulan múltiples procesos biológicos en diferentes tejidos y tipos celulares, que están involucrados en el desarrollo, metabolismo, la cognición, y la inflamación.
Tienen a su vez un alto impacto en la homeostasis energética (aumentando la producción de glucosa en el hígado y promoviendo procesos catabólicos en el músculo, el tejido adiposo y el hueso), así como un efecto inmunosupresor mediante la represión de genes pro-inflamatorios y la activación de genes anti-inflamatorios en diversos tipos celulares del sistema inmune.
Los GRs en la Red NuRCaMeIn
- Receptores nucleares, inflamación y diabetes | Universitat de Barcelona
- Receptores de corticosteroides (GR, MR) y biología de la piel | Instituto de Biomedicina de Valencia IBV-CSIC
Bibliografía
- Cohen DM, Steger DJ. Nuclear Receptor Function through Genomics, Lessons from the Glucocorticoid Receptor. Trends in Endocrinology & Metabolism 2017 Jul;28(7):531-540. doi: 10.1016/j.tem.2017.04.001.
- Ramamoorthy S, Cidlowski JA. Corticosteroids: Mechanisms of Action in Health and Disease. Rheum Dis Clin North Am. 2016 Feb;42(1):15-31, vii. doi: 10.1016/j.rdc.2015.08.002
- Timmermans S, Souffriau J, Libert C. A general introduction to glucocorticoid biology. Front Immunol. 2019;10:1545.doi:10.3389/FIMMU.2019.01545
- Vandewalle J, Luypaert A, De Bosscher K, Libert C. Therapeutic mechanisms of glucocorticoids. Trends Endocrinol Metab. 2018;29:42-54. doi:10.1016/j.tem.2017.10.010
- Weikum ER, Knuesel MT, Ortlund EA, Yamamoto KR. Glucocorticoid receptor control of transcription: precision and plasticity via allostery. Nat Rev Mol Cell Biol. 2017;18:159-174. doi:10.1038/nrm.2016.152
- Jiménez-Panizo A, Alegre-Martí A, et al. The multivalency of the glucocorticoid receptor ligand-binding domain explains its manifold physiological activities. Nucleic Acids Res 2022;gkac1119. doi:10.1093/nar/gkac1119
- Carceller E, Sevilla LM, et al., The mineralocorticoid receptor modulates timing and location of genomic binding by glucocorticoid receptor in response to synthetic glucocorticoids in keratinocytes FASEB J. 2023 Jan;37(1):e22709. doi: 10.1096/fj.202201199RR.
- Bruna A, Nicolàs M, Muñoz A, Kyriakis JM, Caelles C. Glucocorticoid receptor-JNK interaction mediates inhibition of the JNK pathway by glucocorticoids. EMBO J. 2003 Nov 17;22(22):6035-44. doi: 10.1093/emboj/cdg590
