Los “puntos débiles o sensibles” de los ensayos clínicos en niñas/os y en adolescentes
Irene N. Melamed
Médica pediatra y de adolescentes. Miembro de la Comisión Directiva de la
Sociedad Argentina de Salud Integral de la Adolescencia (SASIA), Becaria del
programa de Entrenamiento en Ética de las Investigaciones, FLACSO-Fogarty
2005.
Resumen
La revisión ética de un ensayo clínico1 que incluye a niñas/os y
adolescentes en calidad de participantes, debe centrar su mirada en aspectos
relacionados con la vulnerabilidad inherente a esa etapa de la vida,
condición que se nutre de elementos biológicos, emocionales, de justicia y
de equidad, entre otros.
Sin embargo, la visión sugerida en este caso y sin desoír las
características mencionadas, es la que busca profundizar en uno de los
actores del proceso de investigación: el ensayo clínico.
El objetivo es poder determinar la presencia o no de “zonas frágiles o de
puntos débiles” en su interior, los que al ser individualizados y
especialmente considerados, contribuyan a mejorar la calidad de la revisión
ética de las investigaciones que son llevadas a cabo en niñas/os y
adolescentes.
Palabras clave
Ética de la Investigación; Infancia y Adolescencia; Ensayo Clínico; Vulnerabilidad.
Abstract
The ethical review of clinical research on children and adolescents
should be centered in aspects related to their condition of vulnerability,
which is nurtured by biological, emotional, equity and justice elements.
However, the suggested vision in this case, without overlooking previously
mentioned characteristics, is the one that seeks to delve deeper in one of
the actors of the research process: the clinical research protocol.
The objective is to determine the presence or not of "fragile zones or weak
spots" in its interior, that when individualized and considered, will
contribute to improve the quality of the ethical review on children and
adolescent research.
Key words
Research Ethics; Childhood and Adolescence; Clinical ReSearch; Vulnerability.
Índice
I. Introducción
II. Los “puntos débiles o sensibles” de los ensayos clínicos en niñas/os y adolescentes
II.1. Una mirada al interior de esos puntos débiles
II.2. Los puntos débiles de los ensayos clínicos y la “falsa concepción terapéutica” (Therapeutic Misconception)
III. Aspectos a destacar
IV. Conclusiones
V. Bibliografía
I. Introducción
El escenario de la ética de la investigación en la infancia y en la adolescencia nos confronta en ocasiones con situaciones complejas, en las que no están ausentes numerosas variables y posiciones que a modo de una relación pendular2 oscilan entre la protección y el acceso de niñas/os y adolescentes a las investigaciones, protección que se traduce en la necesidad de adoptar mayores precauciones frente a ciertas condiciones presentes en los protocolos de investigación clínica sometidos a revisión ética en el seno de los Comités de Ética de la Investigación.
El presente artículo tiene el objetivo de bucear así en el interior de uno de los actores del proceso de investigación: el ensayo clínico, a fin de poder identificar en su seno la existencia o no de ciertas condiciones que requieran de miradas adicionales a la hora de su revisión ética.
A este fin describiré lo que denomino “los puntos débiles o sensibles de los ensayos clínicos” que a modo de elementos de cierto conflicto y de tensión pueden encontrarse en la revisión ética de algunos protocolos de investigación por el Comité de Ética de la Investigación, o bien pueden individualizarse a través de la lectura atenta de publicaciones científicas que incluyan investigaciones en niñas/os y adolescentes.
Paralelamente, este artículo tiene el propósito adicional de que sus conclusiones representen un aporte que pueda ser de utilidad en los espacios de formación en temas de Pediatría, ética de la investigación en niñas/os y adolescentes, así como en los debates que se presenten en los Comités de Ética de la Investigación.
II. Los “puntos débiles o sensibles” de los Ensayos Clínicos en niñas/os y adolescentes
La “debilidad o sensibilidad” de un ensayo clínico desarrollado en la infancia y en la adolescencia alude, en mi criterio, a la existencia de una “zona de fragilidad o área gris” en su interior, cuya presencia pueda ser capaz de suscitar conflicto a la hora de su revisión ética, ya sea por ser fuente potencial de uno o más problemas en los sujetos de investigación (niños y adolescentes), así como también en los entornos en los que se lleva a cabo, o en ambos.
El hallazgo de esos puntos débiles o sensibles no persigue ni tiene la voluntad de poner en marcha mecanismos para hacerles frente como si “todo protocolo fuera culpable hasta que se demuestre lo contrario” –en alusión al ámbito del derecho– sino que tiene como objetivo primordial el despertar la mirada más atenta, la que al analizar en profundidad esos puntos débiles nos conduzca finalmente a la construcción de espacios de confianza en el escenario de la ética de la investigación en Pediatría.
La identificación en un ensayo clínico de algunas de esas condiciones de presunta debilidad –las que seguidamente describiré– puede motivar diferentes respuestas que oscilen entre la decisión de que la investigación no deba ser realizada, o bien que pueda serlo, pero con las modificaciones y salvedades consideradas necesarias.
II. 1. Una mirada al interior de los puntos débiles
La “debilidad” de un ensayo clínico, que incluye como participantes de investigación a niñas/os y adolescentes, puede estar determinada por aspectos propios e inherentes al mismo protocolo (ver Figura 1), a sus implicancias y derivaciones, o también la condición de “debilidad” puede estar o no asociada con aspectos que si bien ejerzan influencia sobre el ensayo clínico no pertenezcan ni estén ligadas directamente a él; en ambos casos la condición de sensibilidad o debilidad puede adquirir características cualitativa o cuantitativamente diferentes según se realice en población infantil, adolescente o adulta.
Es de interés mencionar en este entramado de vínculos el caso de los contextos, los que en una estructura relacional con cada protocolo de investigación clínica puedan ser responsables de aportar nuevas otras debilidades o bien de fortalecer negativamente las ya existentes, como lo son las fragmentaciones e inequidades del sistema de salud; se sugiere también el prestar la debida atención a ciertas condiciones de los niños en quiénes se llevará adelante la investigación: edad, desarrollo evolutivo, estado de salud. Todos y cada uno de estos elementos están de algún modo corporizados en la figura que la Dra. Florencia Luna describe como capas de vulnerabilidad3 y acerca de la cuál volveré a lo largo de este escrito por el interés y la importancia que la misma suscita, y porque de algún modo ha sido esta misma “metáfora de las capas” fuerte motivo de inspiración para la presente reflexión.
Sin abandonar la certeza de que los elementos ubicados por fuera de los ensayos clínicos (contextos, vulnerabilidades de las personas) son protagonistas en todo proceso de investigación clínica, es de particular interés a lo largo de este escrito despertar la mirada hacia los aspectos más distintivos e intrínsecos de los ensayos clínicos en niñas/os y adolescentes, los que representan en sí mismos fuente de debilidad.
Es así que considero oportuno seguidamente citar (ver Figura 1) algunas de las condiciones que identificadas puedan aportar a la sensibilidad o a la debilidad de un ensayo clínico en niñas/os y adolescentes y, sin que sea la intención de este material profundizar en cada una de ellas, que su enumeración contribuya a alertar sobre la necesidad de su consideración, para detenerme luego en la búsqueda de ciertas condiciones de debilidad de los ensayos clínicos cuya sola presencia –y a modo aún de una hipótesis exploratoria– puedan o no favorecer la aparición de la “falsa concepción terapéutica” o Therapeutic Misconception4 en el seno de una investigación que incluya niñas/os y adolescentes en calidad de participantes.
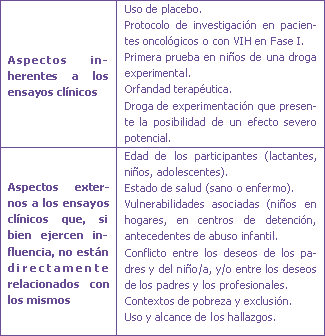
Figura 1. La debilidad de los protocolos: aspectos y condiciones.
Es en este marco en el que la existencia de un grupo control con placebo5, la realización de pruebas de investigación con drogas que son por vez primera probadas en niños, el tipo de procedimiento experimental a utilizar y el potencial daño que la droga en estudio pueda ocasionar, así como también la realización de ensayos clínicos Fase I que buscando responder preguntas acerca de la seguridad de un producto plantea en ocasiones la incertidumbre acerca de un beneficio potencial, representan todas ellas situaciones que pueden cristalizar la aparición de los “puntos débiles o sensibles” de un ensayo clínico, siendo en sí mismas fuente de dificultad a la hora de la revisión ética.
En este sentido la sumatoria de debilidades presente en cada protocolo de investigación clínica puede a su vez ser copartícipe de un mayor número de problemas según la investigación se realice en un país de los denominados centrales, o en vías de desarrollo y es posible que dichas condiciones al igual que otras ameriten la puesta en marcha de uno o más dispositivos que profundizando en la debilidad del protocolo de investigación clínica fortalezcan sus mecanismos de lectura y de revisión.
De este modo la visión que propongo a partir de la identificación de “puntos débiles o sensibles” en los ensayos clínicos, es aquella que sin dejar de lado las vulnerabilidades de las personas/poblaciones intente profundizar e introducirse en esos rasgos distintivos de los protocolos de investigación clínica para que el genuino diálogo6 entre esos diferentes elementos, contribuya a la comprensión y el análisis a los fines de la ética de la investigación.
La reflexión que en mi criterio subyace, en línea con las capas de vulnerabilidad que la investigadora Florencia Luna propone, es si la existencia de “puntos débiles o zonas sensibles” en el marco de un protocolo de investigación clínica en la infancia y en la adolescencia podría significar la aparición de una capa más de vulnerabilidad que incremente o potencie las ya presentes; en este sentido cabe la pregunta: ¿Representan estos puntos débiles variables independientes cuya existencia es autónoma de las capas de vulnerabilidad?, o ¿su presencia misma está determinada por esas capas las que en una suerte de relación casi simbiótica le confieren a esos puntos débiles significados y sentidos?
Avanzando un paso más, ¿es apropiado pensar que todo protocolo de investigación clínica en niños y adolescentes, desde el momento mismo en el que se inicia, registra una tonalidad neutra, la que comienza progresivamente a adquirir matices de grises (capas) y que en ocasiones en vez de iluminarlo lo oscurecen? ¿El hallazgo de esas condiciones de fragilidad (puntos débiles o sensibles) representa un elemento suficiente para la adopción de mayores recaudos?, o ¿es la interacción de esas condiciones entre sí y con los factores inherentes al entorno y a los sujetos mismos (en este caso niñas/os y adolescentes) la que nos interpela a construir nuevas miradas?
Es posible que para los interrogantes anteriores no exista una respuesta única y que para ciertas circunstancias los puntos débiles de los ensayos clínicos a los que hacía referencia se vean potenciados por la existencia de vulnerabilidad en los niños y adolescentes y en los contextos en los que el ensayo clínico se lleve a cabo, mientras que en otros casos ambas variables: sensibilidad del protocolo o puntos débiles y vulnerabilidad de las/os participantes en una investigación, sean variables (si bien relacionadas) independientes en sus respectivos recorridos.
Paralelamente, es de importancia destacar que la existencia de “puntos débiles o sensibles” en todo protocolo de investigación clínica en la etapa infantil y adolescente no supone la obligatoriedad de pensar que el ensayo es “no ético”.
Sin embargo, enfatizo que la identificación de esa debilidad podría actuar como una “bandera roja” (red flags) o señal de alarma que al igual que en el ámbito asistencial nos genere una cierta alerta, en este caso respecto de qué protocolos o ensayos clínicos pueden suponer un mayor desafío a la hora de la revisión y por ende, la puesta en funcionamiento desde el ámbito de los Comités de Ética de la Investigación de una mayor atención.
II. 2. Los puntos débiles de los ensayos clínicos y la “falsa concepción terapéutica” (Therapeutic Misconception)
Considero de particular interés introducirme en la hipótesis exploratoria a la que hacía referencia acerca de si la existencia de ciertas condiciones de los protocolos de investigación clínica (puntos débiles o sensibles) realizados en niñas/os y adolescentes, puede o no favorecer la aparición de la tan temida “falsa concepción terapéutica” o Therapeutic Misconception (en adelante, TM)7 y que de confirmarse, si sería, en efecto, la TM la que le otorgaría a esos atributos negativos de los ensayos clínicos una mayor debilidad en una suerte de retroalimentación positiva.
En relación con la preocupación anterior una lectura posible es que no serían las condiciones de fragilidad de los ensayos clínicos las que podrían contribuir o favorecer la aparición de la “falsa concepción terapéutica”, sino el rol dual que en ocasiones ejerce el profesional que lidera la investigación (investigador/médico asistencial), o también lo serían las características de la entidad mórbida que niñas/os y adolescentes presenten, motivación esta última de importancia para la participación en un ensayo clínico ya sea por propia voluntad o por decisión de sus padres o adultos a cargo. Si esto fuera así, deberíamos no ya centrar la atención en los rasgos de sensibilidad o debilidad que contengan los protocolos de investigación, sino en los roles profesionales así como en las motivaciones de las personas (niños y adolescentes) que son invitadas potencialmente a participar.
A modo aún de una reflexión preliminar es posible que la alteración de la salud que niñas/os y adolescentes presenten deje espacios –a modo de valencias libres– en ellos y/o en sus familias, en donde puedan filtrarse esas condiciones de debilidad de los ensayos clínicos a las que hacía referencia. ¿Es lo mismo la utilización de un placebo en una investigación en una persona con un problema de salud menor o banal, que en aquella cuya única opción posible de hallar un tratamiento pueda ser encontrada en el marco de una investigación? ¿Es el placebo entonces el punto de conflicto, la condición de salud del niño/adolescente, o lo son ambos en interacción?
En este sentido y a modo de ejemplo considero oportuno hacer mención a un tipo de ensayo clínico –que aún guardo en mi memoria– cuyo objetivo era el de probar un medicamento destinado a evitar la aparición del síndrome urémico hemolítico, siendo esta última una entidad para la cuál no existe tratamiento salvo el de las complicaciones en la medida que aparecen. En este caso y al no haber tratamiento disponible el uso del placebo no suponía conflicto ético; la entidad mórbida en esa ocasión se erigía en la principal fuente de motivación para el ingreso de un niño a la investigación: encontrar la “cura” para lo que aún no tiene cura a pesar de los problemas potenciales derivados de esa experimentación.
La utilización de preguntas orientadoras que a modo de un algoritmo bioético contribuya a la comprensión genuina de las motivaciones de las personas, en este caso niñas/os, adolescentes y familias para decidir participar en un protocolo de investigación clínica, representa un recurso adecuado y un factor de enriquecimiento que aporte al debate desde las primeras etapas en las que se planifica toda investigación.
Otro punto débil o sensible de los ensayos clínicos situado ya no en su interior sino por fuera de ellos y que merece especial consideración, es el que está relacionado con el uso y el alcance de los hallazgos luego de su difusión a través de las diferentes publicaciones, lo cuál abre un abanico de posibilidades y de nuevas preguntas en relación con la necesidad incuestionable de producir y de acceder al conocimiento en forma libre y los riesgos que en ocasiones y paralelamente supone la difusión de algunos resultados.
Este último elemento lejos de querer desalentar la realización de investigaciones por su potencial uso dual, debe profundizar la mirada aguda que anticipe situaciones problemáticas o de dificultad a fin de poder superarlas.
III. Aspectos a destacar
Uno de los objetivos primordiales de este escrito ha sido el de poder reflexionar en torno a un actor esencial en la revisión ética de toda investigación en la infancia y en la adolescencia: el ensayo clínico, y en particular en su independencia o no de las condiciones de vulnerabilidad de los niños y adolescentes así como de los contextos.
En este sentido, y en consonancia con la “metáfora de las capas” que la Dra. Luna propone, considero de interés –en una suerte de diálogo con la investigadora– dejar planteados nuevos interrogantes acerca de si esos “puntos débiles o sensibles” de los protocolos en niñas/os y adolescentes pueden ser pensados como una nueva capa adicional de vulnerabilidad, o si las mismas vulnerabilidades (capas) al entrar en contacto con el ensayo clínico son las que le otorgan a esas áreas o zonas sensibles una mayor visibilidad.
Paralelamente, la identificación de ciertas y determinadas condiciones presentes en los protocolos de investigación clínica en niños y adolescentes pasibles de promover la aparición de la Therapeutic Misconception ha sido otro elemento que a lo largo de este recorrido buscó despertar la atención de los lectores; si bien no he realizado un abordaje en profundidad de la TM, sugiero a los fines de su prevención focalizar más que en las condiciones intrínsecas de los ensayos clínicos –los puntos débiles o sensibles– aunque no excluyo su importancia, en una etapa anterior, particularmente en las motivaciones que conducen a una familia a incorporar a un niña/o en una investigación.
IV. Conclusiones
Pareciera ser entonces que en todo ensayo clínico existe una diversidad de elementos a considerar, no sólo al interior del proceso sino desde las etapas previas y posteriores a su realización, en coincidencia con la difusión responsable de los resultados.
En esta misma línea, el propósito adicional de este material ha sido el de contribuir a que las investigaciones no sean consideradas en forma aislada sino en el marco de un verdadero ciclo de vida de todo proyecto, en la que cada etapa de ese ciclo pueda determinar y/o favorecer el desarrollo satisfactorio de los ensayos clínicos y, para que cada una de las “zonas débiles o sensibles” que puedan estar presentes se vea fortalecida a través de la perspectiva ética, la que a modo de una genuina malla o red de contención sea el sustento del respeto y la confianza en escenarios de investigación.
Agradecimientos: Un especial agradecimiento a la Dra Florencia Luna, generosa interlocutora fuente de inspiración, a la Dra. María Casado, Directora del Máster en Bioética y Derecho de la UB por iluminar nuevas miradas, a Itziar Lecuona, Albert Royes y Fabiola Leyton, por el estímulo y acompañamiento, así como al equipo de profesionales del Comité Editorial por contribuir a través de la interesante y enriquecedora orientación, a la publicación de este escrito en este espacio.
Bibliografía
- Buxó M Jesús. “Dialogar la nanoética”, Revista de Bioética y Derecho, 2008; 12 pag 12.
- Joffe, S, Fernandez, C. y Pentz,
R. “Involving Children with Cancer in Decision Making about Research
Participation”, J.
Pediatrics, 2006; 149: 862-868.
http://download.journals.elsevierhealth.com/pdfs/journals/0022-3476/PIIS0022347606007840.pdf.
- Kodish, Eric, Ethics and Research with Children, Oxford University Press, 2005; pag 8.
- Kodish, Eric, Ethics and Research with Children, Oxford University Press, 2005; pag 295.
- Luna, F, “Elucidating the Concept of Vulnerability. Layers not Labels”, IJFAB, vol. 2: 1, 2009.
- Mastroianni, Anna y Jeffrey, Kahn, "Swinging on the Pendulum: Shifting Views of Justice in Human Subjects Research", en Hastings Center Report 21, 3 (2001): 21-28 http://www.thehastingscenter.org.
- Sociedad Española de Farmacología Clínica, en http://www.se-fc.org/0301.php.
Notas
1. Las autoridades reguladoras españolas de acuerdo con el artículo 58 de la Ley 29/2006 de garantías y uso racional de los medicamentos y productos sanitarios de 26 julio de 2006 y el artículo 2 del Real Decreto 223/2004 de 6 de febrero de 2004 entienden por Ensayo Clínico: “ toda investigación efectuada en seres humanos, con el fin de determinar o confirmar los efectos clínicos, farmacológicos, y/o demás efectos farmacodinámicos, y/o de detectar las reacciones adversas, y/o de estudiar la absorción, distribución, metabolismo y eliminación de uno o varios medicamentos en investigación con el fin de determinar su seguridad y/o su eficacia ”. El carácter experimental del ensayo clínico obliga al investigador a considerar tres dimensiones: la metodológica o científica, la ética y la normativa o reguladora ya que se hace necesario proteger la integridad de los pacientes y sus derechos así como la fiabilidad de los datos, Sociedad Española de Farmacología Clínica, en http://www.se-fc.org/0301.php.
2. Mastroianni, Anna y Jeffrey, Kahn, "Swinging on the Pendulum: Shifting Views of Justice in Human Subjects Research", en Hastings Center Report 21, 3 (2001): 21-28.
3. Florencia Luna describe la Metáfora de las Capas, Elucidating the Concept of Vulnerability, Layers not Labels, The International Journal of Feminist Approaches to Bioethics Vol .2 N 1, 2009, en la que examina el rol de las “etiquetas” en el marco de la ética de la investigación y propone y desarrolla un mecanismo dinámico que contribuya a la comprensión del concepto de vulnerabilidad. La metáfora de las capas en palabras de la investigadora ofrece la idea de algo que puede ser (…)” más flexible y que puede ser removido de uno en uno, capa por capa. No hay una “sólida y única vulnerabilidad” que agote la categoría, pueden haber diferentes vulnerabilidades, diferentes capas operando”(…).
4. Therapeutic Misconception o Falsa Concepción Terapéutica alude a la existencia de confusión respecto del verdadero propósito de la investigación en la que en ocasiones las/os participantes creen que el tratamiento y la investigación están ambos regidos por el mismo objetivo primario: avanzar en los mejores intereses de la persona individual (Appelbaum, Roth & Lidz, 1982) en Kodish E, Ethics and Research with Children, A Case Based Approach, Oxford University Press, 2005 pag 8.
5. Placebo es una denominación que deriva del latín “agradar”. Técnicamente es una sustancia inactiva que se utiliza para remedar una sustancia activa. En el contexto de investigación el uso de placebos puede estar destinado a reducir sesgos y puede ayudar a distinguir entre los efectos farmacológicos verdaderos de los falsos de una intervención experimental, en Kodish E, Ethics and Research with Children, A Case Based Approach, Oxford University Press, 2005 pag 295.
6. Considero de interés hacer mención al artículo de María Jesús Buxó Rey “Dialogar la nanoética”, Revista de Bioética y Derecho, 12, Enero 2008, pag 12, quién destaca las vías y las actividades que se promueven para desplegar el diálogo nanosociedad y que estimo que pueden ser de importancia a los fines de contribuir al encuentro dialógico y hacerlo extensivo a otros aspectos que conciernen a la ética de la investigación.
7. Joffe y Weeks establecen que la “Therapeutic misconception" (TM) constituye la amenaza de mayor importancia a la validez del consentimiento informado en investigación y se preguntan si cualquier manifestación de TM entre las/los participantes de investigaciones invalida el consentimiento a participar en la investigación volviendo al reclutamiento como no ético. (Ver Joffe, S.; Weeks, J. C. “Views of American Oncologists about the purpose of medical trials”, J. Natl Cancer Institute 2002;94:1847-1853).
 El contenido de la revista está bajo licencia Creative Commons Reconocimiento - NoComercial - SinObraDerivada (by-nc-nd): No se permite un uso comercial de la obra original ni la generación de obras derivadas.
El contenido de la revista está bajo licencia Creative Commons Reconocimiento - NoComercial - SinObraDerivada (by-nc-nd): No se permite un uso comercial de la obra original ni la generación de obras derivadas.
